Для поліпшення роботи сайту ми використовуємо файли cookie. Продовжуючи переглядати сайт, ви погоджуєтеся з цим.
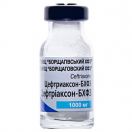
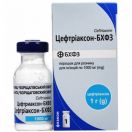
Цефтріаксон-БХФЗ порошок для розчину 1000 мг флакон №1
33,70 ₴
Борщагівський ХФЗ ЗАТ НВЦ (Україна, Київ)


Арт.
7547

У список
Цефтріаксон-БХФЗ порошок для розчину 1000 мг флакон №1 Борщагівський ХФЗ ЗАТ НВЦ (Україна, Київ)
Борщагівський ХФЗ ЗАТ НВЦ (Україна, Київ)
Залишилися питання?
Ми раді допомогти
Характеристики товара
| Виробник | Борщагівський ХФЗ ЗАТ НВЦ (Україна, Київ) |
|---|---|
| Дозування | 1000 мг |
| Головний медикамент | Цефтріаксон |
| Форма товару | Порошок |
| Ознака | Вітчизняний |
| Штрих-код | 4823012512806 |
| Бренд | Цефтриаксон |
| Умови відпуску | за рецептом |
| Призначення | Антибактеріальні засоби |
| Температура зберiгання | не вище 25°C |
Інструкція надана держ. реєстром мед. препаратів України

Перевірено: Громадська Яна

Перевірено: Кортунова Юлія
Оновлено: 13.11.2024
Перевірено
Інструкція
Цефтріаксон-БХФЗ (Ceftriaxone-BCPP) інструкція по застосуванню
Склад
Діюча речовина: цефтріаксон;
- 1 флакон містить цефтріаксон (у вигляді цефтріаксону стерильної натрієвої солі) 500 мг або 1000 мг.
Лікарська форма
Порошок для ін'єкцій.
Основні фізико-хімічні властивості
Кристалічний порошок майже білого або жовтуватого кольору, трохи гігроскопічний.
Фармакотерапевтична група
Антибактеріальні засоби для системного використання. Інші ця-лактамні антибіотики. Цефалоспорини ІІІ покоління. Цефтріаксон. Код ATX J01D D04.
Фармакологічні властивості
Фармакодинаміка
Цефтріаксон – напівсинтетичний антибіотик групи бета-лактамів, цефалоспорин ІІІ покоління; виявляє бактерицидну дію, механізм якого пов'язаний з пригніченням активності ферменту транспептидази, порушенням біосинтезу пептидоглікану клітинної стінки мікроорганізмів; має широкий спектр дії.
Активний щодо грампозитивних аеробів: Staphylococcus aureus (включаючи штами, які продукують пеніциліназ), Staphylococcus epidermidis, Streptococcus pneumoniae, бета-гемолітичних стрептококів групи А (S. pyogenes), Стрепокок. неентерококової групи D ; грамнегативних аеробів: E.coli, H.influenzae, H. parainfluenzae, Klebsiella spp. (включаючи K.pneumoniae), Morganella morganii, Neisseria gonorrhoeae (включаючи штами, що продукують пеніциліназ), Neisseria meningitidis, Proteus mirabilis, Proteus vulgaris, Providencia spp., Pseudomonas aeruginosa, Salmonella (У т.ч. S.typhi), Serratia spp. (включаючи S.marcescens), Shigella spp., Yersinia spp. (У т.ч. Y.enterocolitica), Treponema pallidum; анаеробів: Bacteroides spp. (включаючи деякі штами B.fragilis), Clostridium spp. (проте більшість штамів C.difficile мають резистентність), Peptococcus spp., Peptostreptococcus spp., Fusobacterium spp. (крім F.mortiferum та F.varium).
Препарат активний щодо мікроорганізмів, стійких до пеніцилінів, цефалоспоринів перших поколінь, аміноглікозидів.
До дії препарату стійкі: стафілококи, резистентні до метициліну; більшість штамів ентерококів (у тому числі S.faecalis) та стрептококи групи D; багато штамів бета-лактамазопродукуючих Bacteroides spp. (B.fragilis).
Фармакокінетика
Після внутрішньом'язового введення біодоступність цефтріаксону становить 100%, його максимальна концентрація в плазмі визначається через 2-3 години.
Після введення препарат швидко проникає у тканинну рідину, де протягом 24 годин підтримуються бактерицидні концентрації щодо чутливих мікроорганізмів. Цефтріаксон оборотно зв'язується з альбумінами плазми. Це зв'язування пропорційно концентрації: наприклад, при концентрації препарату в сироватці крові менше 100 мг/л зв'язування цефтріаксону з білками становить 95%, а при концентрації 300 мг/л - тільки 85%. Завдяки нижчому вмісту альбумінів в інтерстиціальній рідині концентрація цефтріаксону в ній вища, ніж у сироватці крові.
Цефтріаксон добре проникає в органи та рідини організму (перитонеальну, плевральну, спинномозкову, синовіальну), в кісткову тканину, проникає через плаценту, у невеликій кількості (3-4%) проникає у грудне молоко. При менінгіті у дітей, у тому числі новонароджених препарат проникає в запалення мозкові оболонки, при цьому концентрація його в цереброспінальній рідині становить 17% від концентрації в плазмі крові.
Препарат виділяється у незміненому вигляді на 50-60% нирками та 40-50% – з жовчю. При нирковій недостатності фармакокінетика майже не змінюється, спостерігається лише незначне збільшення періоду напіввиведення. При порушенні функції нирок збільшується виділення з жовчю, і якщо є патологія печінки, то збільшується виділення цефтриаксона нирками. Період напіввиведення у здорових дорослих становить близько 8 годин, у новонароджених до 8 днів та у людей віком від 75 років збільшується у 2-3 рази.
Клінічні властивості
Показання
Інфекційно-запальні захворювання, спричинені чутливими до препарату мікроорганізмами:
- інфекції дихальних шляхів, особливо пневмонія, а також інфекції вуха, горла та носа;
- інфекції органів черевної порожнини (перитоніт, інфекції жовчовивідних шляхів та шлунково-кишкового тракту);
- інфекції нирок та сечовивідних шляхів;
- інфекції статевих органів, включаючи гонорею;
- сепсис;
- інфекції кісток, суглобів, м'яких тканин, шкіри, а також ранові інфекції;
- інфекції у хворих з ослабленим імунним захистом;
- менінгіт;
- дисемінований бореліоз Лайма (II та III стадії).
Періопераційна профілактика інфекцій при хірургічних втручаннях на органах шлунково-кишкового тракту, жовчовивідних шляхів, сечовивідних шляхів та гінекологічних процедур, але тільки у випадках потенційної чи відомої контамінації.
При призначенні цефтріаксону слід дотримуватись офіційних рекомендацій щодо антибіотикотерапії та рекомендацій щодо профілактики антибіотикорезистентності.
Протипоказання Цефтріаксону-БХФЗ
Гіперчутливість до цефтріаксону, до будь-якого антибіотика цефалоспоринового ряду, до лідокаїну (внутрішньом'язове введення).
Наявність в анамнезі тяжких реакцій гіперчутливості (наприклад, анафілактичних реакцій) до будь-якого іншого типу бета-лактамних антибактеріальних засобів (пеніцилінів, монобактамів, карбапенемів).
Недоношені новонароджені до 41 тижня з урахуванням терміну внутрішньоутробного розвитку (гестаційний вік + календарний вік)*.
Доношені новонароджені (віком до 28 днів життя):
- з гіпербілірубінемією, жовтяницею, з гіпоальбумінемією, ацидозом (за цих станів зв'язування білірубіну з білками крові знижується)*;
- при необхідності (або очікується, що потребуватимуть) внутрішньовенного введення препаратів кальцію або кальцієвмісних розчинів через ризик утворення преципітатів цефтріаксону – кальцію в легенях та нирках (див. розділи «Особливості застосування» та «Побічні реакції»).
* У дослідженнях іn vitro було показано, що цефтріаксон може витісняти білірубін із зв'язку з альбуміном сироватки крові, що призводить до можливого ризику розвитку білірубіну. енцефалопатії у таких пацієнтів.
Перед внутрішньом'язовим введенням цефтріаксону слід обов'язково виключити наявність протипоказань до застосування лідокаїну, якщо його застосовують як розчинник (див. розділ «Особливості застосування» та інструкцію з медичного застосування лідокаїну, особливо протипоказання).
Розчини цефтріаксону, що містять лідокаїн, ніколи не слід вводити внутрішньовенно.
Взаємодія з іншими лікарськими засобами та іншими видами взаємодій.
Препарати кальцію. Через ризик виникнення преципітатів кальцієвих солей цефтріаксону Не слід застосовувати розчини кальцію, такі як розчин Рінгера або розчин Гартмана, для відновлення препарату у флаконах або для подальшого розведення відновленого розчину для внутрішньовенного введення.
Преципітати цефтріаксону - кальцію також можуть утворюватися при змішуванні цефтріаксону з кальційвмісними розчинами в одній інфузійній системі.
Цефтріаксон не можна вводити одночасно з внутрішньовенними кальцієвмісними розчинами, в т. ч. з кальційвмісними розчинами для тривалих інфузій, такими як розчини для парентерального живлення, за допомогою Y-подібної системи. Однак усім пацієнтам, за винятком новонароджених, цефтріаксон і кальцієвмісні розчини можна вводити послідовно, один після одного, якщо між інфузіями ретельно промити інфузійну систему сумісною рідиною. У дослідженнях і n vitro з використанням плазми крові дорослих та плазми пуповинної крові новонароджених було показано, що у новонароджених існує підвищений ризик утворення преципітатів цефтріаксону-кальцію (див. розділи «Спосіб застосування та дози», «Протипоказання», «Особливості застосування», « Побічні реакції»).
Немає повідомлень про взаємодію між цефтріаксоном та пероральними кальцієвмісними препаратами, про взаємодію між цефтріаксоном при внутрішньом'язовому застосуванні та кальцієвмісними препаратами, які застосовують внутрішньовенно або перорально.
Нестероїдні протизапальні засоби, антиагреганти, антагоністи вітаміну К (такі як варфарин). Підвищення ризику кровотеч. Посилення ефекту антагоністів вітаміну К. Рекомендується частий контроль міжнародного нормалізованого співвідношення (МНС) та відповідне коригування доз антагоністів вітаміну К під час та після застосування цефтріаксону (див. «Побічні реакції»).
Аміноглікозиди. Наявні дані про потенційне посилення токсичного впливу аміноглікозидів на нирки при їх застосуванні разом із цефалоспоринами суперечливі. У таких випадках у клінічній практиці слід ретельно моніторувати рівень аміноглікозидів та функцію нирок.
При необхідності комбінованого лікування слід вводити препарати в різні місця та не змішувати в одному шприці або в одному розчині для інфузії через фізико-хімічну несумісність.
Бактеріостатичні антибіотики (хлорамфенікол, тетрацикліни). Можливе зниження бактерицидного ефекту цефтріаксону.
У дослідженні in vitro при застосуванні хлорамфеніколу у поєднанні з цефтріаксоном спостерігалися антагоністичні ефекти. Клінічна значимість цих даних невідома.
Інші бета-лактамні антибіотики. Можливий розвиток перехресних алергічних реакцій.
Петльові діуретики. При одночасному застосуванні високих доз цефтріаксону та потужних діуретиків (наприклад, фуросеміду) порушень функції нирок не спостерігалось.
Пробенецид. Не впливає на тубулярну секрецію цефтріаксону (на відміну інших цефалоспоринів).
Гормональні контрацептиви. Як і при застосуванні інших антибіотиків, знижується ефективність гормональних контрацептивів, тому рекомендується використовувати додаткові (негормональні) методи контрацепції під час лікування та 1 місяць після його завершення.
Етанол. Не спостерігалося ефектів, схожих дію дисульфирама. Цефтріаксон не містить N - метилтіотетразольну групу, яка могла б викликати непереносимість етанолу або кровотечу, що властиво деяким іншим цефалоспоринам.
Подібно до інших антибіотиків, цефтр та аксон може знижувати терапевтичний ефект вакцини проти тифу, проте такий ефект поширюється тільки на ослаблений штам Ty21.
Речовини, які використовуються при лабораторних аналізах. Можливий хибно-позитивний результат реакції на глюкозу в сечі при застосуванні розчину Бенедикту або Фелінгу.
Цефтріаксон несумісний і його не можна змішувати в одній ємності або одночасно вводити з амсакрином, ванкоміцином, флуконазолом, аміноглікозидами.
Особливості застосування препарату
Реакції гіперчутливості
Як і при застосуванні інших цефалоспоринів та бета-лактамних антибіотиків, повідомлялося про випадки важких гострих реакцій гіперчутливості, іноді з летальним кінцем, навіть якщо у докладному анамнезі не було відповідних даних. При розвитку таких реакцій застосування препарату слід негайно припинити та ввести адреналін (епінефрін), глюкокортикоїди, вжити інших належних невідкладних заходів.
Перед початком лікування пацієнта слід розпитати про наявність в анамнезі тяжких реакцій гіперчутливості до цефтріаксону, інших цефалоспоринів, інших бета-лактамних антибіотиків. Існує ймовірність перехресних алергічних реакцій між пеніцилінами та цефалоспоринами. З обережністю слід застосовувати цефтріаксон пацієнтам з наявністю в анамнезі легкої гіперчутливості до інших бета-лактамних препаратів.
При застосуванні цефтріаксону зареєстровані випадки таких тяжких побічних реакцій з боку шкіри, як синдром Стівенса-Джонсона, синдром Лайєлла (токсичний епідермальний некроліз) та DRESS-синдром (медикаментозна висипка з еозинофілією та системними проявами), які можуть становити загрозу життю; проте частота цих явищ невідома (див. розділ «Побічні реакції»).
Реакція Яриша-Герксгеймера
У деяких пацієнтів з інфекціями, викликаними спірохетами, може розвинутись реакція Яриша-Герксгеймера невдовзі після початку лікування цефтріаксоном. Реакція Яриша-Герксгеймера зазвичай є самообмежувальним станом або може вимагати симптоматичного лікування. Якщо розвинулася така реакція, лікування антибіотиком припиняти не слід.
Взаємодія з кальцієвмісними препаратами
Описано випадки утворення преципітатів кальцієвої солі цефтріаксону в легенях та нирках з летальним кінцем у недоношених та доношених немовлят до 1 місяця. Щонайменше одному з цих пацієнтів вводили цефтріаксон і кальцій у різний час і через різні внутрішньовенні інфузійні системи. В даний час не зареєстровано підтверджених випадків утворення внутрішньосудинних. преципітатів у пацієнтів, крім випадків у новонароджених, яким вводили цефтріаксон і кальцієвмісні розчини або інші кальцієвмісні препарати. У дослідженнях in vitro було показано, що новонароджені мають підвищений ризик утворення преципітатів кальцієвої солі цефтріаксону порівняно з пацієнтами іншого віку.
Пацієнтам будь-якого віку цефтріаксон не слід змішувати або одночасно вводити разом з будь-якими кальцієвмісними внутрішньовенними розчинами, навіть при використанні різних інфузійних систем або при введенні препаратів у різні інфузійні ділянки.
Однак пацієнтам віком від 28 днів цефтріаксон і кальційвмісні розчини можна вводити послідовно, один після одного, при введенні препаратів через різні інфузійні системи в різні ділянки тіла або заміни/ретельного промивання інфузійної системи між введенням цих засобів фізіологічним сольовим розчином, щоб запобігти утворенню. Пацієнтам, які потребують безперервних інфузій кальцієвмісних розчинів для повного парентерального харчування (ППХ), лікар може призначити альтернативне антибактеріальне лікування, не пов'язане з подібним ризиком утворення преципітатів. Якщо застосування цефтріаксону пацієнтам, які потребують ППХ, визнано необхідним, розчини для ППХ та цефтріаксон можна вводити одночасно, але через різні інфузійні системи та різні ділянки тіла. Крім того, введення розчинів для ППХ можна призупинити на час інфузії цефтріаксону та промити інфузійні системи між введенням розчинів (див. розділи «Протипоказання», «Побічні реакції» та «Несумісність»).
Діти
Безпека та ефективність цефтріаксону у новонароджених, новонароджених та дітей були встановлені при застосуванні доз, описаних у розділі «Спосіб застосування та дози». Цефтріаксон, як і деякі інші цефалоспорини, може витісняти білірубін через сироватковий альбумін.
Цефтріаксон протипоказаний недоношеним та доношеним новонародженим із ризиком розвитку білірубінової енцефалопатії (див. розділ "Протипоказання").
Імуноопосередкована гемолітична анемія
Повідомлялося про випадки гемолітичної анемії імунопосередкованої у пацієнтів, які отримували цефалоспорини, включаючи цефтріаксон (див. розділ «Побічні реакції»). Тяжкі випадки гемолітичної анемії (в т.ч. з летальним кінцем) були зареєстровані протягом лікування цефтріаксоном як у дорослих, так і у дітей. У разі розвитку анемії при лікуванні препаратом слід розглянути можливість діагнозу та скасувати антибіотик для визначення етіології анемії.
Тривале лікування
Протягом тривалого лікування препаратом рекомендується регулярно контролювати розгорнутий анал із крові.
Коліт/надмірне зростання нечутливих мікроорганізмів
Про випадки антибіотико-асоційованого коліту/псевдомембранозного коліту повідомлялося при застосуванні багатьох антибактеріальних засобів, включаючи цефтріаксон. Ступінь тяжкості проявів може коливатися від легкого до загрозливого життя, тому важливо розглядати можливість цього діагнозу у всіх пацієнтів, у яких під час або після застосування цефтріаксону виникла діарея (див. розділ «Побічні реакції»). Може знадобитися припинення терапії цефтріаксоном та застосування специфічної терапії проти Clostridium. difficile. Лікарські засоби, що пригнічують перистальтику, не слід застосовувати.
Як і при застосуванні інших антибактеріальних засобів, можливий розвиток суперінфекції, спричиненої нечутливими до препарату мікроорганізмами.
Тяжка ниркова та печінкова недостатність
У разі тяжкої ниркової та печінкової недостатності рекомендується ретельний клінічний моніторинг безпеки та ефективності препарату (див. «Спосіб застосування та дози»).
Вплив на результати серологічних досліджень
При застосуванні цефтріаксону тест Кумбса може давати хибно-позитивні результати. Також цефтріаксон може призводити до хибно-позитивних результатів при проведенні проби на галактоземію, при визначенні глюкози в сечі неферментативними методами. Тому протягом лікування цефтріаксоном рівні глюкози у сечі слід визначати за допомогою ферментативних методів аналізу (див. розділ «Побічні реакції»).
Натрію
Кожен грам препарату містить 3,6 ммоль (83,03 мг) натрію, що необхідно враховувати пацієнтам, які дотримуються дієти з контрольованим вмістом натрію.
Антибактеріальний діапазон
Цефтріаксон має обмежений спектр антибактеріальної активності і може бути непридатним для монотерапії при певних типах інфекції, крім випадків, коли збудник вже підтверджений (див. «Спосіб застосування та дози»). У разі полімікробних інфекцій, коли серед підозрюваних збудників є резистентними до цефтріаксону, слід розглянути необхідність застосування додаткових антибіотиків.
Застосування лідокаїну
Якщо як розчинник застосовують розчин лідокаїну, цефтріаксон можна вводити тільки внутрішньом'язово. Перед введенням препарату слід обов'язково врахувати протипоказання до застосування лідокаїну, застереження та іншу відповідну інформацію, наведену в інструкції з медичного застосування лідокаїну (див. розділ «Протипоказання»). Розчин лідокаїну в жодному разі не можна вводити внутрішньовенно.
Жовчокам'яна хвороба
У разі наявності на сонограмі тіней слід врахувати можливість утворення преципітатів кальцієвої солі цефтріаксону. Тіні, які були помилково прийняті за жовчні камені, спостерігалися на сонограмах жовчного міхура і частіше виявлялися при застосуванні цефтріаксону у дозі 1 г на добу та вище. Особливої обережності слід дотримуватись при застосуванні препарату дітям. Такі преципітати зникають після припинення терапії цефтріаксоном. Зрідка утворення преципітатів кальцієвої солі цефтріаксон супроводжувалося симптоматикою. Ризик утворення преципітатів зростає при тривалості лікування, що перевищує 14 днів, при нирковій недостатності, зневодненні або парентеральному харчуванні. За наявності симптомів рекомендується консервативне нехірургічне лікування. Лікар повинен розглянути питання про припинення застосування препарату з огляду на оцінку співвідношення користь/ризик у кожному конкретному випадку (див. розділ «Побічні реакції»).
Жовчний стаз
При застосуванні цефтріаксону було зареєстровано випадки панкреатиту, спричинені обструкцією жовчних шляхів. Більшість пацієнтів мали фактори ризику розвитку холестазу та біліарного злажу, наприклад: попередня значна терапія, тяжка хвороба, повне парентеральне харчування. Не можна виключати, що тригером або кофактором цього ускладнення може бути утворення жовчних шляхів преципітатів внаслідок застосування цефтріаксону.
Нирковокам'яна хвороба
Зареєстровано випадки утворення ниркового каміння, що зникало після припинення застосування цефтріаксону (див. «Побічні реакції»). За наявності симптомів слід провести ультразвукове обстеження. Рішення про застосування препарату пацієнтам з наявністю в анамнезі ниркового каміння або гіперкальціурії приймає лікар з огляду на оцінку співвідношення користь/ризик у кожному конкретному випадку.
Енцефалопатія
Повідомлялося про розвиток енцефалопатії при застосуванні цефтріаксону (див. розділ Побічні реакції), особливо у пацієнтів похилого віку з тяжкою нирковою недостатністю (див. Спосіб застосування та дози) або розладами центральної нервової системи. Якщо є підозра на цефтріаксон – асоційовану енцефалопатію (наприклад, зниження рівня свідомості, зміна психічного стану, міоклонію, судоми), слід розглянути питання про припинення застосування цефтріаксону.
Утилізація лікарського засобу
Надходження лікарського засобу до зовнішнього середовища слід звести до мінімуму. Слід запобігати попаданню лікарського засобу до каналізаційної системи або домашніх відходів. Невикористаний лікарський засіб після закінчення лікування або терміну придатності слід повернути в оригінальній упаковці постачальнику (лікарю чи фармацевту) для правильної утилізації.
Застосування у період вагітності або годування груддю
Вагітність
Цефтріаксон проникає крізь плацентарний бар'єр. Дані про застосування вагітним жінкам обмежені. Під час вагітності, зокрема у І триместрі, цефтріаксон можна застосовувати лише якщо користь перевищує ризик.
Годування груддю
Цефтріаксон проникає в грудне молоко в низьких концентраціях, але при застосуванні препарату в терапевтичних дозах не очікується жодного впливу на немовлят. Однак не можна виключати ризик розвитку діареї та грибкової інфекції слизових. Слід враховувати можливість сенсибілізацію. Необхідно ухвалити рішення про припинення годування груддю або припинення/відмову від застосування цефтріаксону з урахуванням користі від грудного вигодовування для дитини та користі від терапії для жінки.
Фертильність
У дослідженнях репродуктивної функції не виявлено ознак небажаного впливу на чоловічу чи жіночу фертильність.
Здатність впливати на швидкість реакції при керуванні автотранспортом чи іншими механізмами
Відповідних досліджень не проводили. Цефтріаксон може впливати на здатність керувати транспортними засобами або іншими механізмами, оскільки можливе виникнення таких побічних реакцій, як запаморочення.
Спосіб застосування та дози Цефтріаксон-БХФЗ
Перед початком терапії необхідно виключити наявність у пацієнта підвищеної чутливості до антибіотика та лідокаїну (у разі внутрішньом'язового способу введення), зробивши шкірну пробу.
Добове дозування для дорослих та дітей віком від 12 років становить 1 2 г препарату 1 раз на добу (кожні 24 години). При тяжких інфекціях або інфекціях, збудники яких мають лише помірну чутливість до цефтріаксону, добову дозу можна збільшувати до 4 г. При дозах, що перевищують 2 г на добу, можливе введення препарату 2 рази на добу (кожні 12 годин).
Діти
Новонароджені (віком до 14 днів) та недоношені діти (від 41 тижня скоригованого віку): 20-50 мг/кг маси тіла. 1 раз на добу протягом не менше 60 хвилин для попередження витіснення білірубіну із зв'язку з альбумінами крові та зменшення потенційного білірубінового ризику енцефалопатії. Зважаючи на недорозвиненість ферментної системи, добова доза не повинна перевищувати 50 мг/кг маси тіла. При визначенні дози для доношених і недоношених дітей відмінностей немає.
Цефтріаксон протипоказаний для застосування новонародженим ( віком ≤ 28 днів) у випадках, якщо існує (або очікується) необхідність лікування внутрішньовенними кальцієвмісними розчинами, в т.ч. при постійних внутрішньовенних кальцієвмісних інфузіях, як, наприклад, парентеральне харчування, через ризик виникнення преципітатів. цефтріаксону - кальцію (див. розділ "Протипоказання").
Діти віком від 15 днів до 12 років: 20-80 мг/кг маси тіла 1 раз на добу. Дозування понад 80 мг/кг маси тіла слід уникати (за винятком випадків менінгіту) через підвищення ризику розвитку жовчних преципітатів.
Дітям з масою тіла більше 50 кг призначай дози, як для дорослих.
Внутрішньовенні дози 50 мг/кг маси тіла або вище слід вводити шляхом краплинної інфузії, повільно принаймні 30 хвилин.
Пацієнти похилого віку: дози відповідають дозам для дорослих; корекція доз не потрібна при задовільній функції печінки та нирок.
Тривалість лікування Цефтріаксон залежить від перебігу захворювання
Застосування препарату слід продовжувати (як і будь-яку антибіотикотерапію) протягом 48-72 годин після зникнення симптомів захворювання та підтвердження ефекту лікування результатами бактеріологічного аналізу.
Комбінована терапія
Існують дані про синергізм при одночасному застосуванні цефтріаксону та аміноглікозидів щодо багатьох грамнегативних мікроорганізмів. Незважаючи на те, що підвищену ефективність таких комбінацій не завжди можна припустити, її слід мати на увазі за наявності важких інфекцій, що загрожують життю, викликаних Pseudomonas aeruginosa. Через фізичну несумісність цефтріаксону та аміноглікозидів слід вводити окремо у рекомендованих дозах.
Дозування в особливих випадках
При бактеріальному менінгіті у немовлят та дітей віком від 15 днів до 12 років лікування починати з дози 100 мг/кг маси тіла (але не більше 4 г) 1 раз на добу. Після ідентифікації збудника та визначення його чутливості дозу можна зменшити відповідно. Для новонароджених до 2 тижнів не слід перевищувати 50 мг/кг/добу.
Найкращі результати досягалися за такої тривалості лікування:
- Neisseria meningitidis - 4 дні
- Haemophilus influenzae - 6 днів
- Streptococcus pneumoniae - 7 днів
- Бореліоз Лайма: дорослим та дітям – 50 мг/кг (найвища добова доза – 2 г) 1 раз на день протягом 14 днів.
- Гонорея (викликана штамами, що утворюють і не утворюють пеніциліназ): рекомендується призначати разову дозу 250 мг внутрішньом'язово.
Профілактика інфекцій у хірургії
Для профілактики післяопераційних інфекцій при контамінованих або потенційно контамінованих хірургічних втручаннях рекомендується вводити одноразово за 30-90 хвилин до початку операції. При операціях на товстій та прямій кишці рекомендується вводити одночасно (але окремо) препарат одного з 5-нітроімідазолів (наприклад, орнідазол).
Пацієнтам із порушенням функції нирок при нормальній функції печінки немає необхідності знижувати дозу препарату. Тільки при нирковій недостатності у передтермінальній стадії (кліренс креатиніну менше 10 мл/хв) добова доза не повинна перевищувати 2 г.
Пацієнти, які перебувають на гемодіалізі, не вимагають додаткового введення препарату після діалізу. Слід контролювати концентрацію цефтру та аксону у сироватці крові для можливої корекції дози, оскільки у цих пацієнтів може знижуватись швидкість його виведення.
Добова доза цефтріаксону для пацієнтів, які перебувають на гемодіалізі, не повинна перевищувати 2 г.
Пацієнтам з порушенням функції печінки при нормальній функції нирок немає необхідності знижувати дозу.
При одночасній тяжкій нирковій та печінковій недостатності слід регулярно визначати концентрацію цефтріаксону в плазмі крові та за необхідності проводити корекцію дози, оскільки швидкість виведення цефтріаксону може знижуватися.
Приготування розчинів
Розчини готують перед застосуванням. Після додавання розчинника візуально слід оцінити повноту розчинення. Залежно від концентрації та тривалості зберігання колір розчинів може варіювати від блідо-жовтого до жовтого. Ця властивість активної речовини не впливає на ефективність чи переносимість препарату.
Цефтр іаксон застосовувати внутрішньовенно або внутрішньом'язово. Внутрішньовенне введення слід розглядати, якщо внутрішньовенний шлях введення неможливий або менш придатний для пацієнта. Дози ≥ 2 г слід вводити внутрішньовенно.
Внутрішньом'язова ін'єкція
Для внутрішньом'язової ін'єкції вміст флакону з 0,5 г цефтріаксону слід розчинити у 2 мл 1% розчину лідокаїну, вміст флакону з 1 г – у 3,5 мл 1% розчину лідокаїну (після попередньо проведеної проби на чутливість до лідокаїну).
Розчин слід вводити глибоко всередину щодо великої м'язової маси, трохи більше 1 придатного ділянки.
Розчин, що містить лідокаїн, не можна вводити внутрішньовенно! (Див. розділ «Протипоказання»). Для детальної інформації необхідно ознайомитись з інструкцією з медичного застосування лідокаїну.
Внутрішньовенне введення
Для внутрішньовенних ін'єкцій вміст флакона з 0,5 г слід розчинити в 5 мл води для ін'єкцій, вміст флакона з 1 г - в 10 мл води для ін'єкцій. Вводити повільно протягом 2-4 хвилин.
Внутрішньовенна інфузія повинна тривати не менше 30 хвилин. Для приготування розчину 2 г цефтріаксон слід розчинити в 40 мл одного з нижченаведених інфузійних розчинів, що не містять іонів кальцію:
- 0,9% розчин хлориду натрію;
- 5% розчин глюкози;
- 0,45% розчин хлориду натрію + 2,5% розчин глюкози;
- 10% розчин глюкози;
- 6% розчин декстрану в 5% розчині глюкози;
- стерильна вода для ін'єкцій.
Враховуючи можливу несумісність, розчини, що містять цефтріаксон, не можна змішувати з розчинами, що містять інші антибіотики, як при приготуванні, так і при введенні.
Однак 2 г цефтріаксону та 1 г орнідазол фізично та хімічно сумісні у 250 мл 0,9% розчину натрію хлориду або розчину глюкози.
Не можна використовувати розчинники, які містять кальцій, такі як розчин Рінгера або розчин Гартмана, для відновлення цефтріаксону у флаконах або для розведення відновленого розчину для внутрішньовенного введення, оскільки можливе утворення преципітатів. цефтріаксону – кальцію.
Виникнення преципітатів Цефтріаксон -кальція також можлива при змішуванні цефтріаксону з кальцієвмісними розчинами в одній інфузійній системі. Таким чином, цефтріаксон не можна вводити внутрішньовенно одночасно з кальцієвмісними розчинами, в т.ч. год. з кальцієвмісними розчинами для тривалих інфузій, такими як розчини для парентерального живлення, через Y-подібний у систем. Однак усім пацієнтам, за винятком новонароджених, цефтріаксон і кальційвмісні розчини можна вводити послідовно, якщо інфузійну систему ретельно промити між інфузіями сумісним розчином (див. Взаємодія з іншими лікарськими засобами та інші види взаємодій).
Свіжоприготовані розчини зберігають свою фізичну та хімічну стабільність протягом 8 годин при температурі 25°С та протягом 24 годин при температурі 2-8°С.
Діти
Препарат застосовувати дітям згідно з дозуванням, зазначеним у розділі «Спосіб застосування та дози».
Передозування
Симптоми: нудота, блювання, діарея, посилення побічних реакцій.
Лікування: проводити симптоматичну та підтримуючу терапію. Гемодіаліз і перитонеальний діаліз неефективні (не зменшують через їх концентрацію і препарату в плазмі крові). Специфічного антидоту немає.
Побічні реакції Цефтріаксону-БХФЗ
Травний тракт: рідкий стілець/діарея, диспепсія, нудота, блювання, стоматит, глосит, дисгевзія, біль у животі, зниження апетиту (зазвичай помірно виражені, проходять протягом/після припинення лікування); панкреатит (можливо, через обструкцію жовчовивідних шляхів).
Гепатобіліарна система: преципітація кальцієвих солей цефтріаксону у жовчному міхурі*; підвищення рівня білірубіну, активності печінкових трансаміназ, лужної фосфатази у плазмі крові, дисфункція печінки, гепатит 1, холестатичний гепатит 1,2, ядерна жовтяниця.
Система кровотворення: еозинофілія, лейкопенія, нейтропенія, лімфопенія, тромбоцитопенія, гранулоцитопенія, анемія, включаючи гемолітичну анемію, подовження протромбінового часу, епістаксис, коагулопатію, агранулоцитоз (зазвичай після 10 днів лікування та сумування).
Нервова система: біль голови, запаморочення, можливі судомні напади, енцефалопатія.
Органи слуху та рівноваги: вертиго.
Сечовидільна система: підвищення рівня креатиніну в крові, циліндрурія, глюкозурія, гематурія, олігурія, утворення преципітатів. цефтріаксону у нирках (зазвичай оборотне), анурія, ниркова недостатність, гострий тубулярний некроз.
Шкіра та підшкірна клітковина: підвищене потовиділення, припливи, алергічні шкірні реакції (в т.ч. кропив'янка, дерматити, макулопапульозний висип або екзантема), свербіж, мультиформна ексудативна еритема, синдром Стівенса-Дйсона DRESS - синдром (медикаментоз ), гостра генералізована екзантематозний пустульоз.
Імунна система: реакції гіперчутливості, анафілактичний шок, анафілактичні реакції, анафілактоїдні реакції, сироваткова хвороба, реакція Яриша-Герксгеймера.
Дихальні розлади: бронхоспазм, алергічні пневмоніти.
Інфекції та інвазії: можливі мікози статевих органів, розвиток суперінфекції, псевдомембранозний коліт.
Загальні розлади та реакції у місці введення препарату: флебіт/тромбофлебіт при внутрішньовенному введенні, біль та/або інфільтрат у місці введення, медикаментозна лихоманка, набряки шкіри та суглобів, озноб.
Лабораторні аналізи: гіперазотемія, можуть відзначатися хибнопозитивні результати реакції Кумбса, проби на галактоземію, щодо глюкози в сечі неферментативними методами.
1 Зазвичай має оборотний характер у разі припинення прийому цефтриаксона.
2 Див. розділ «Особливості застосування»
Інфекції та інвазії
Випадки діареї після застосування цефтріаксону можуть бути пов'язані з надмірним зростанням Clostridium difficile.
Тактика лікування повинна включати введення адекватної кількості рідини та електролітів (див. розділ «Особливості застосування»).
* Преципітати кальцієвої солі цефтріаксону.
Рідкісні випадки тяжких побічних реакцій, іноді з летальним кінцем, зареєстровані у недоношених та доношених новонароджених (вік <28 днів), яким внутрішньовенно вводили цефтріаксон та препарати кальцію. При аутопсії у легенях та нирках були виявлені преципітати кальцієвої солі цефтріаксону. Високий ризик утворення преципітатів у новонароджених є наслідком малого об'єму крові у них та довшого, ніж у дорослих, періоду напіввиведення. цефтріаксона (див. розділи "Протипоказання", "Особливості застосування").
Зареєстровані випадки утворення преципітатів у нирках, переважно у дітей віком від 3 років, які отримували великі добові дози (≥ 80 мг/кг/добу), або при кумулятивній дозі понад 10 гі мали додаткові фактори ризику (обмежене вживання рідини, дегідратація, обмеження рухомості). режим). Освіта преципітатів може супроводжуватися симптомами або бути асимптомним, може призводити до ниркової недостатності та анурії. Преципітати зникають після припинення застосування цефтріаксону (див. розділ «Особливості застосування»).
Зареєстровані випадки утворення преципітатів кальцієвої солі цефтріаксону в жовчному міхурі, переважно у пацієнтів, яким препарат вводили у дозах вище за стандартну рекомендовану дозу. Діти, за даними проспективних досліджень цефтриаксона, частота освіти преципітатів при внутрішньовенному введенні була різною – у деяких дослідженнях понад 30%. При повільному введенні препарату (протягом 20-30 хвилин) частота утворення преципітатів очевидно нижча. Освіта преципітатів зазвичай не супроводжується симптомами, але в окремих випадках виникали такі клінічні симптоми, як біль, нудота і блювання. У таких випадках рекомендується симптоматичне лікування. Після припинення застосування цефтріаксону преципітати зазвичай зникають (див. розділ «Особливості застосування»).
Повідомлення про підозрювані побічні реакції.
Повідомлення про підозрювані побічні реакції після реєстрації лікарського засобу має велике значення. Це забезпечує постійний моніторинг співвідношення користь/ризик лікарського засобу. Медичним працівникам слід повідомляти про будь-які підозрювані побічні реакції відповідно до законодавства.
Термін придатності
3 роки.
Умови зберігання
В оригінальній упаковці за температури не вище 25 °С.
Зберігати у недоступному для дітей місці.
Несумісність
Не змішувати з іншими лікарськими засобами в одному шприці або системі внутрішньовенного введення.
Фармацевтично несумісний з іншими антимікробними засобами. Не допускається змішувати розчин препарату в одній ємності з іншими антибіотиками, з розчинами, що містять кальцій (наприклад, розчини Гартмана і Рінгера).
Несумісний із амсакрином, ванкоміцином, флуконазолом, лабеталолом, аміноглікозидами, іншими антибіотиками.
Упаковка
Порошок розчину для ін'єкцій по 500 мг. По 1 флакон з порошком; по 1 флакону у пачці; по 1 флакон з порошком у комплекті з розчинником (вода для ін'єкцій) по 5 мл у ампулі в пачці з картонною перегородкою.
Порошок для розчину для ін'єкцій по 1000 мг. По 1 флакон з порошком; по 1 флакону у пачці; по 1 флакон з порошком у комплекті з розчинником (вода для ін'єкцій); по 5 мл або 10 мл в ампулі в пачці з картонною перегородкою; по 1 флакону з порошком у комплекті з розчинником (лідокаїну) гідрохлорид, розчин для ін'єкцій (10 мг/мл) по 3,5 мл у ампулі в пачці з картонною перегородкою.
Категорія відпуску з аптеки
За рецептом.
- Склад
- Лікарська форма
- Фармакотерапевтична група
- Фармакологічні властивості
- Показання
- Протипоказання Цефтріаксону-БХФЗ
- Особливості застосування препарату
- Спосіб застосування та дози Цефтріаксон-БХФЗ
- Передозування
- Побічні реакції Цефтріаксону-БХФЗ
- Термін придатності
- Умови зберігання
- Упаковка
- Категорія відпуску з аптеки
Відгуки користувачів
Цей продукт ще не має відгуків.
Залишити відгук
Дивіться інші товари у категорії:
Смекта смекта ціна Цефтриаксон цефтриаксон ціна цефтриаксон порошок дитячий антибіотик цефікс Цинкіт Мілістан синус магніюсульфат порошок синусан квамател флакон аспірин порошок гриппостад порошок комбігрип порошок субалін флакон німедар порошок дексалгін порошок бетаргін порошок ворміл порошок лінекс дитячий порошок пробіз ціна
Зверніть увагу
Інформація/інструкція до препарату носить ознайомчий характер і призначена виключно для інформаційних цілей.